氢冶金原理与未来
2022-11-18
郭汉杰,郭靖
北京科技大学
1氢冶金的发展和目前的问题
目前媒体上关于氢冶金的报道。







学者建议和发文




目前的问题
1 大家都看好氢冶金的前景,没有实质性的研发,哪怕是理论模型计算,更多停留在概念上;
2 冷静考虑,氢来自何方?如何来?有多少?
3 近期和远期的实施步骤是什么?其依据?
2 高炉碳冶金的原理解析
高炉碳还原----用热力学的两个模型从另外角度看高炉运行
(1)热力学模型一
Fe2O3碳还原最理想的热力学模型
在等温等压下,热力学体系中 ,组元数C=6:Fe2O3、CO、CO2、O2、Fe、C;
元素数m=3:Fe、C、O,体系中独立的化学反应数: r=c-m=3 。
因此从热力学理论上用3个独立化学反应描述氧化铁的碳还原的始态和末态实际上就反映了全部的工艺过程。

此二反应构成铁矿石Fe2O3与碳的还原炼铁最理想的模型(以下简称为模型一)。其中作为还原过程能源C的消耗分为两个部分:
1)按照反应(1)还原的化学计量关系,还原1Kg铁(或吨铁)所需要的碳素,为最为理想的还原剂用量;
2)由碳的完全燃烧反应(2)提供给还原反应(1)必须的化学热所消耗的碳素;
3)以上两个反应产生的还原煤气的组成CO、CO2,由完成反应(1)及(2)的化学计量算出。
以还原1KgFe(或1000KgFe)为基准模拟计算高炉状态下,碳素还原纯Fe2O3的反应,由于这个反应是吸热反应,所以要完成这个反应需要给高炉下部吹氧,碳氧反应放热维持表观的直接还原。



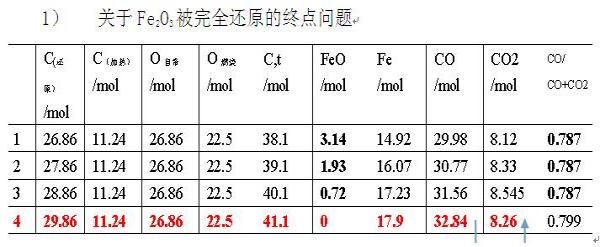
按照模型一(1#)的理想计算所得的碳、氧的配加量,代入最小自由能模型二进行精确计算,发现此时并不能完全得到1Kg(17.9mol)的铁,只得到了833gFe(14.92mol),体系中还有226g FeO(3.14mol)没有被还原。在此基础上,逐渐增加还原剂C,见2#、3#、4#,每增加1molC,FeO逐渐减小,直至4#时消失。4#时总耗碳42.1mol,1Kg(17.9mol)的铁完全被还原出来。
为什么模型二的结果与热力学的化学计量结果不一致?

……

相关文章
[错误报告] [推荐] [收藏] [打印] [关闭] [返回顶部]

 已有
已有


